
CRISPRa-SCREEN服务
一、CRISPRa-SCREEN简介
CRISPRa-SCREEN 又称 CRISPR-Cas9 转录激活文库筛选,或基因激活文库筛选。该系统灵活方便,为研究基因功能提供了极为便利的工具。
研究基因功能时,一般采用RNAi基因敲减、Cas9基因敲除做出基因功能缺失的表型,额外转入基因表达质粒,产生基因激活表型。通过比较缺失表型和过表达表型的生物功能特性分析基因功能。对于比较大的基因以及难以克隆的基因,比如部分受体和通道蛋白编码序列可以达到10kb以上。构建基因表达质粒会很困难,因此很难做出过表达的功能表型。
现在,CRISPR-Cas9也被应用于基因组水平的功能获得型(gain-of-function,GOF)遗传筛选。CRISPR synergistic activation mediator (SAM) 系统可以通过导入几个简单的原件,即可实现对任何一个基因的特异性激活,从而避开了基因克隆和构建复杂表达载体的难题。亘安生物推出的 CRISPR 转录激活 (CRISPRa)文库筛选服务,为通过功能获得性基因调控,探索治疗药物的耐药机制提供了新的机会。
二、原理流程
CRISPR SAM采用切割活性缺失的dCas9蛋白融合VP64转录激活蛋白,加上能与RNA结合蛋白MS2的sgRNA,特异性识别并结合目标基因的启动子。MS2蛋白上连接p65和HSF1转录激活蛋白。通过多种转录激活蛋白的协同作用,能更好的模拟细胞内转录激活,激活目标基因的转录【1】。
SAM系统包含三部分组件:
1,细胞核定位的催化活性缺失dCas9与VP64激活域的融合蛋白,NLS-dCas9-VP64。
2,修改的sgRNA骨架,在四环区(tetraloop)和茎环2区(stem loop 2)加入两个发卡结构适配子(hairpin aptamer),可以结合二聚化的MS2噬菌体外壳蛋白。
3,MS2与p65和人类热激转录因子HSF1转录激活域的融合蛋白,MS2-p65-HSF1。
CRISPRa-SCREEN流程:
CRISPR-Cas9 SAM系统有三部分,因此需要先构建稳定表达SAM系统的细胞系。以MOI<1将NLS-dCas9-VP64 和MS2-p65-HSF1慢病毒转染目标细胞(此步骤也可以将sgRNA表达框与dCas9-VP64构建在同一个载体骨架中,则只需先构建稳定表达MS2-p65-HSF1的细胞系),进行抗生素筛选,筛选完成后得到稳定表达dCas9-VP64 和MS2-p65-HSF1的细胞系,以MOI≈0.3将SAM sgRNA慢病毒文库转染上述筛选完成的细胞,抗生素筛选后,达到约每个sgRNA有500个细胞覆盖;根据实验目的进行小分子,药物或其他条件处理后,分离DNA,扩增DNA,NGS建库测序,数据分析。
注意:包装完成的sgRNA慢病毒文库以比较低的MOI如0.3转染目标细胞,经过抗生素筛选,尽量使每个细胞仅接受一个拷贝的sgRNA,即每个细胞仅有一个目标基因被过表达;转染细胞的数量建议每条sgRNA>500个细胞。
三、CRISPRa-SCREEN应用
这种新颖的全基因组CRISPRa平台可以在内源背景中增强基因表达,以研究与基因激活相关的效应,并可以有效地鉴定与我们的CRISPRi功能缺失筛选中鉴定的那些基因互补的耐药基因,为您发现潜在的治疗靶点提供支持。利用经过CRISPR筛选专家优化的CRISPRa文库,我们可以进行准确的功能获得性基因筛选。
CRISPR 激活 (CRISPRa) 筛选提供了研究基因功能增益的能力,以拓宽药物发现和开发项目的可能应用范围。通过利用没有活性的 Cas9 (dCas9),它保留了与 DNA 结合的能力,但不具有催化活性,可以实现基因表达的调控,从而提供高度精确和灵敏的功能获得性筛选解决方案。
与CRISPRi筛选相结合,CRISPRa筛选可以揭示在感兴趣药物存在的情况下,当激活或抑制时表现出相反效应的“开关”样基因,从而让我们更加接近发现明确治疗靶点的前景。
它的主要应用包括:
1、在全基因组范围内研究基因功能获得性的效应
2、通过研究基因功能获得性表型来探索药物与基因的相互作用
3、使用反向功能同源工具验证基因功能缺失效应
4、与CRISPRi筛选相结合进行基因网络分析
5、针对非蛋白编码区域(例如lncRNA)靶点进行研究
应用案例分享:
1. 药物作用机制的研究:Genome-scale transcriptional activation by an engineered CRISPR-Cas9 complex
在顽固的疾病治疗中,常常有病人对治疗药物产生先天或后天的抗药性。因此,在基因组水平理解哪些基因会影响药物的功效能够为临床治疗提供更准确的方案。Konermann等【3】应用SAM转录激活文库在A375(BRAF(V600E))黑色素瘤细胞中筛选抵抗黑色素瘤药物(BRAF inhibitor,PLX-4720)的基因位点。该研究构建了基因组水平的SAM sgRNA慢病毒文库,包含70290个sgRNAs,靶定RefSeq数据库中23430个coding isoforms转录起始位点上游200 bp位置,每个基因设计3个sgRNAs。通过文库筛选,NGS分析和验证,最终鉴定到一系列已知的和新的参与PLX-4720抗药性相关的候选基因。
2. 长链非编码RNA功能研究:Genome-scale activation screen identifies a lncRNA locus regulating a gene neighborhood 哺乳动物基因组包含成千上万个可以转录长的非编码RNA(long noncoding RNAs,lncRNA)的基因座,其中一些已知在多种细胞过程中起关键调控作用。尽管lncRNAs可能以反式(in trans, act non-locally)的方式起作用,但也有证据表明,许多lncRNAs以顺势(in cis, act locally)的方式参与调控,即该基因座的lncRNA会对附近基因的表达起调控作用。然而,直到目前,对lncRNA功能和机制的研究仍充满挑战。为了探索该问题,Joung等【5】构建了基因组水平上靶定10000多个lncRNA转录起始位点的sgRNA慢病毒文库,并利用SAM转录激活系统在黑色素瘤细胞中筛选鉴定到11个新的介导BRAF抑制剂(vemurafenib)抗性的lncRNA基因座。对其中一个候选基因:EMICERI 进行详细功能分析发现,该lncRNA的转录激活导致四个相邻蛋白质编码基因的剂量依赖性激活,并且其中一个蛋白编码基因导致了BRAF抑制剂抗性表型。该研究为系统的探索非编码RNA的功能提供了参考。
四、平台介绍
我们的 CRISPR 激活筛选平台基于我们行业领先、高度复杂的 CRISPR KO 筛选平台。该 CRISPRa 筛选平台经过多年内部领先专家的优化,提供了强大的筛选解决方案,可灵活满足您的需求。亘安生物提供定制化CRISPRa文库筛选服务,包括转录激活sgRNA的设计,质粒构建及NGS质检、慢病毒包装、SAM系统稳定表达细胞系、细胞筛选实验后NGS测序分析,交付客户分析报告,为客户提供一站式服务。
质量标准:
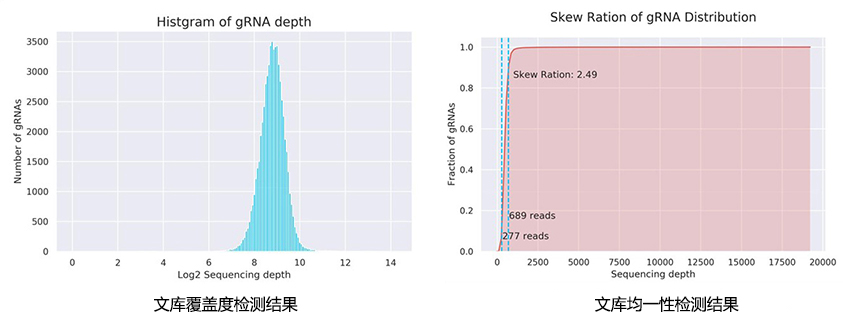
1.sgRNA质粒文库覆盖度可以达到99%以上,NGS测序进行覆盖度、均一性等的检测质控,测序深度300-500X,均一性小于8;
2.文库质粒交付1mg,浓度一般默认1ug/ul以上,酶切后条带单一,纯度90%以上,但是由于是质粒库,有一定几率出现较弱的诡带,这是文库制备阶段无法避免的情况,包病毒会过滤掉,使用的是凯杰去内毒素试剂盒提取;
3.慢病毒交付标准,滴度不低于8TU/mL;
4.文库筛选实验需根据客户具体要求寄实验实际情况进行评估。
五、优势特点
1、BI设计,公认的sgRNA评分标准、优化的设计算法批量设计sgRNA
2、可设计任意NCBI数据库中存在的物种或基因的sgRNA,可一次设计上万条sgRNAs
3、可定制特定物种全基因组文库和亚文库
4、高通量测序分析,高质检标准和丰富的生信经验
5、质粒文库构建,高覆盖度高均一性,覆盖度:≥99%
6、Oligo Pool合成可达300nt,高保真性高均一性,均一性:<8
7、质粒总量:≥500 μg(无内毒素)
8、NGS测序深度:≥300x
9、病毒包装,高滴度高质检标准
10、细胞筛选,高筛选标准和完善的筛选平台
参考文献:
[1] Joung, Julia, et al. "Genome-scale CRISPR-Cas9 knockout and transcriptional activation screening." Nature protocols 12.4 (2017): 828-863.
[2] Cruz, Cristina, et al. "A gain-of-function screen identifying genes required for growth and pattern formation of the Drosophila melanogaster wing." Genetics 183.3 (2009): 1005-1026.
[3] Konermann, Silvana, et al. "Genome-scale transcriptional activation by an engineered CRISPR-Cas9 complex." Nature 517.7536 (2015): 583-588.
[4] Chavez, Alejandro, et al. "Comparison of Cas9 activators in multiple species." Nature methods 13.7 (2016): 563-567.
[5] Joung, Julia, et al. "Genome-scale activation screen identifies a lncRNA locus regulating a gene neighbourhood." Nature 548.7667 (2017): 343-346.
CRISPRa-SCREEN 又称 CRISPR-Cas9 转录激活文库筛选,或基因激活文库筛选。该系统灵活方便,为研究基因功能提供了极为便利的工具。
研究基因功能时,一般采用RNAi基因敲减、Cas9基因敲除做出基因功能缺失的表型,额外转入基因表达质粒,产生基因激活表型。通过比较缺失表型和过表达表型的生物功能特性分析基因功能。对于比较大的基因以及难以克隆的基因,比如部分受体和通道蛋白编码序列可以达到10kb以上。构建基因表达质粒会很困难,因此很难做出过表达的功能表型。
现在,CRISPR-Cas9也被应用于基因组水平的功能获得型(gain-of-function,GOF)遗传筛选。CRISPR synergistic activation mediator (SAM) 系统可以通过导入几个简单的原件,即可实现对任何一个基因的特异性激活,从而避开了基因克隆和构建复杂表达载体的难题。亘安生物推出的 CRISPR 转录激活 (CRISPRa)文库筛选服务,为通过功能获得性基因调控,探索治疗药物的耐药机制提供了新的机会。
二、原理流程
CRISPR SAM采用切割活性缺失的dCas9蛋白融合VP64转录激活蛋白,加上能与RNA结合蛋白MS2的sgRNA,特异性识别并结合目标基因的启动子。MS2蛋白上连接p65和HSF1转录激活蛋白。通过多种转录激活蛋白的协同作用,能更好的模拟细胞内转录激活,激活目标基因的转录【1】。
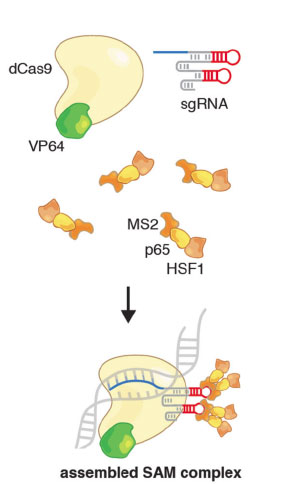
SAM系统包含三部分组件:
1,细胞核定位的催化活性缺失dCas9与VP64激活域的融合蛋白,NLS-dCas9-VP64。
2,修改的sgRNA骨架,在四环区(tetraloop)和茎环2区(stem loop 2)加入两个发卡结构适配子(hairpin aptamer),可以结合二聚化的MS2噬菌体外壳蛋白。
3,MS2与p65和人类热激转录因子HSF1转录激活域的融合蛋白,MS2-p65-HSF1。
CRISPRa-SCREEN流程:
CRISPR-Cas9 SAM系统有三部分,因此需要先构建稳定表达SAM系统的细胞系。以MOI<1将NLS-dCas9-VP64 和MS2-p65-HSF1慢病毒转染目标细胞(此步骤也可以将sgRNA表达框与dCas9-VP64构建在同一个载体骨架中,则只需先构建稳定表达MS2-p65-HSF1的细胞系),进行抗生素筛选,筛选完成后得到稳定表达dCas9-VP64 和MS2-p65-HSF1的细胞系,以MOI≈0.3将SAM sgRNA慢病毒文库转染上述筛选完成的细胞,抗生素筛选后,达到约每个sgRNA有500个细胞覆盖;根据实验目的进行小分子,药物或其他条件处理后,分离DNA,扩增DNA,NGS建库测序,数据分析。
注意:包装完成的sgRNA慢病毒文库以比较低的MOI如0.3转染目标细胞,经过抗生素筛选,尽量使每个细胞仅接受一个拷贝的sgRNA,即每个细胞仅有一个目标基因被过表达;转染细胞的数量建议每条sgRNA>500个细胞。
三、CRISPRa-SCREEN应用
这种新颖的全基因组CRISPRa平台可以在内源背景中增强基因表达,以研究与基因激活相关的效应,并可以有效地鉴定与我们的CRISPRi功能缺失筛选中鉴定的那些基因互补的耐药基因,为您发现潜在的治疗靶点提供支持。利用经过CRISPR筛选专家优化的CRISPRa文库,我们可以进行准确的功能获得性基因筛选。
CRISPR 激活 (CRISPRa) 筛选提供了研究基因功能增益的能力,以拓宽药物发现和开发项目的可能应用范围。通过利用没有活性的 Cas9 (dCas9),它保留了与 DNA 结合的能力,但不具有催化活性,可以实现基因表达的调控,从而提供高度精确和灵敏的功能获得性筛选解决方案。
与CRISPRi筛选相结合,CRISPRa筛选可以揭示在感兴趣药物存在的情况下,当激活或抑制时表现出相反效应的“开关”样基因,从而让我们更加接近发现明确治疗靶点的前景。
它的主要应用包括:
1、在全基因组范围内研究基因功能获得性的效应
2、通过研究基因功能获得性表型来探索药物与基因的相互作用
3、使用反向功能同源工具验证基因功能缺失效应
4、与CRISPRi筛选相结合进行基因网络分析
5、针对非蛋白编码区域(例如lncRNA)靶点进行研究
应用案例分享:
1. 药物作用机制的研究:Genome-scale transcriptional activation by an engineered CRISPR-Cas9 complex
在顽固的疾病治疗中,常常有病人对治疗药物产生先天或后天的抗药性。因此,在基因组水平理解哪些基因会影响药物的功效能够为临床治疗提供更准确的方案。Konermann等【3】应用SAM转录激活文库在A375(BRAF(V600E))黑色素瘤细胞中筛选抵抗黑色素瘤药物(BRAF inhibitor,PLX-4720)的基因位点。该研究构建了基因组水平的SAM sgRNA慢病毒文库,包含70290个sgRNAs,靶定RefSeq数据库中23430个coding isoforms转录起始位点上游200 bp位置,每个基因设计3个sgRNAs。通过文库筛选,NGS分析和验证,最终鉴定到一系列已知的和新的参与PLX-4720抗药性相关的候选基因。
2. 长链非编码RNA功能研究:Genome-scale activation screen identifies a lncRNA locus regulating a gene neighborhood 哺乳动物基因组包含成千上万个可以转录长的非编码RNA(long noncoding RNAs,lncRNA)的基因座,其中一些已知在多种细胞过程中起关键调控作用。尽管lncRNAs可能以反式(in trans, act non-locally)的方式起作用,但也有证据表明,许多lncRNAs以顺势(in cis, act locally)的方式参与调控,即该基因座的lncRNA会对附近基因的表达起调控作用。然而,直到目前,对lncRNA功能和机制的研究仍充满挑战。为了探索该问题,Joung等【5】构建了基因组水平上靶定10000多个lncRNA转录起始位点的sgRNA慢病毒文库,并利用SAM转录激活系统在黑色素瘤细胞中筛选鉴定到11个新的介导BRAF抑制剂(vemurafenib)抗性的lncRNA基因座。对其中一个候选基因:EMICERI 进行详细功能分析发现,该lncRNA的转录激活导致四个相邻蛋白质编码基因的剂量依赖性激活,并且其中一个蛋白编码基因导致了BRAF抑制剂抗性表型。该研究为系统的探索非编码RNA的功能提供了参考。
四、平台介绍
我们的 CRISPR 激活筛选平台基于我们行业领先、高度复杂的 CRISPR KO 筛选平台。该 CRISPRa 筛选平台经过多年内部领先专家的优化,提供了强大的筛选解决方案,可灵活满足您的需求。亘安生物提供定制化CRISPRa文库筛选服务,包括转录激活sgRNA的设计,质粒构建及NGS质检、慢病毒包装、SAM系统稳定表达细胞系、细胞筛选实验后NGS测序分析,交付客户分析报告,为客户提供一站式服务。
质量标准:

1.sgRNA质粒文库覆盖度可以达到99%以上,NGS测序进行覆盖度、均一性等的检测质控,测序深度300-500X,均一性小于8;
2.文库质粒交付1mg,浓度一般默认1ug/ul以上,酶切后条带单一,纯度90%以上,但是由于是质粒库,有一定几率出现较弱的诡带,这是文库制备阶段无法避免的情况,包病毒会过滤掉,使用的是凯杰去内毒素试剂盒提取;
3.慢病毒交付标准,滴度不低于8TU/mL;
4.文库筛选实验需根据客户具体要求寄实验实际情况进行评估。
五、优势特点
1、BI设计,公认的sgRNA评分标准、优化的设计算法批量设计sgRNA
2、可设计任意NCBI数据库中存在的物种或基因的sgRNA,可一次设计上万条sgRNAs
3、可定制特定物种全基因组文库和亚文库
4、高通量测序分析,高质检标准和丰富的生信经验
5、质粒文库构建,高覆盖度高均一性,覆盖度:≥99%
6、Oligo Pool合成可达300nt,高保真性高均一性,均一性:<8
7、质粒总量:≥500 μg(无内毒素)
8、NGS测序深度:≥300x
9、病毒包装,高滴度高质检标准
10、细胞筛选,高筛选标准和完善的筛选平台
参考文献:
[1] Joung, Julia, et al. "Genome-scale CRISPR-Cas9 knockout and transcriptional activation screening." Nature protocols 12.4 (2017): 828-863.
[2] Cruz, Cristina, et al. "A gain-of-function screen identifying genes required for growth and pattern formation of the Drosophila melanogaster wing." Genetics 183.3 (2009): 1005-1026.
[3] Konermann, Silvana, et al. "Genome-scale transcriptional activation by an engineered CRISPR-Cas9 complex." Nature 517.7536 (2015): 583-588.
[4] Chavez, Alejandro, et al. "Comparison of Cas9 activators in multiple species." Nature methods 13.7 (2016): 563-567.
[5] Joung, Julia, et al. "Genome-scale activation screen identifies a lncRNA locus regulating a gene neighbourhood." Nature 548.7667 (2017): 343-346.



