
高通量蛋白质组学研究服务
蛋白质组(Proteome)是指基因组表达的所有相应蛋白质的集合,即细胞、组织或机体全部蛋白质的存在及其活动方式,最早是由澳大利亚科学家Wilkins和Williams于1994年提出。蛋白质组学(Proteomics)是指利用高分辨的蛋白质分离技术和高效的蛋白质鉴定技术在蛋白质水平上整体性、动态和定量地研究生命现象及规律的科学,是系统生物学的有机组成部分,是一门大规模、高通量、系统化的研究某一类型细胞组织、某一基因组所表达的所有蛋白质,包括组成蛋白质一级结构的氨基酸序列,蛋白质的丰度,蛋白质的翻译后修饰(PTM)以及蛋白质之间的相互作用的学科。
蛋白质组是空间和时间上动态变化着的整体,相比稳定的基因组,蛋白质组是遗传信息、环境因素、生活习惯等多因素的综合体现。蛋白质组是最能实时反映细胞/组织功能和疾病发生状态的一类分子,也是疾病发生最相关的分子类型,具有广阔研究前景。
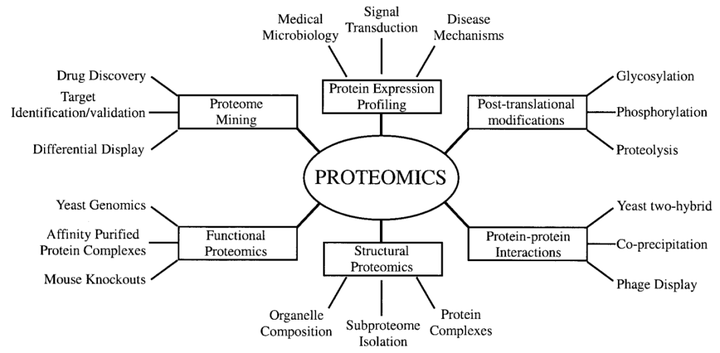
根据研究目的和手段的不同,蛋白质组研究主要包括三个方面:
● 表达蛋白质组学:组织样品中主要蛋白质、不同组织样品差异表达蛋白质的鉴定。
● 结构蛋白质组学:蛋白复合物结构、亚细胞蛋白质组分析。
● 功能蛋白质组学:蛋白质功能相关信号、机制、蛋白互作信息研究分析。
二、原理流程
1. 研究的主要内容
1.1. 蛋白质定性:鉴定特定细胞、组织或器官的蛋白质种类(蛋白质组全谱鉴定)。蛋白质组学的核心内容之一就是蛋白质鉴定。传统的方法如蛋白质微量测序、氨基酸组成分析(如Edman降解法)费时费力、通量低,存在不容易实现规模化和自动化,结果灵敏度差等问题。当前主流的基于软电离技术的液相色谱-质谱系统(Liquid Chromatography-Mass Spectrometry,LC-MS/MS)是实现高通量蛋白组全谱鉴定的主要方法。
1.2. 蛋白质定量:研究特定条件下蛋白质的表达量变化(定量蛋白质组学)。例如在许多疾病的发生和发展进程中,常常伴随着某些蛋白质的表达异常。定量蛋白质组学就是把一个基因组表达的全部蛋白质或一个复杂的混合体系中所有的蛋白质进行精确的定量和鉴定。定量蛋白质组学技术主要分为标记(Label)和非标记(Label free)定量策略,标记策略又分为体内标记(SILAC)和体外标记(iTRAQ)两种。
1.3. 蛋白质功能:明确蛋白质在生命活动中执行的功能(功能蛋白质组学),揭示蛋白质之间复杂的相互作用机制(相互作用蛋白质组学)。如分析酶活性和确定酶底物,细胞因子的生物分析/配体-受体结合分析。可以利用基因敲除和反义技术分析基因表达产物——蛋白质的功能,另外对蛋白质表达出来后在细胞内的定位研究也在一定程度上有助于蛋白质功能的了解。
1.4. 蛋白质结构:研究蛋白质精确的二维、三维甚至四维结构(结构蛋白质组学)以及蛋白质翻译后修饰(修饰蛋白质组学)。通过理论研究计算推导预测蛋白质的空间结构,或者探索蛋白质在结构变化过程中各种光学、物理学等特征变化来了解蛋白质结构信息。利用液相色谱-质谱系统(LC-MS/MS)结合数据库检索的方法,实现对目前所有已知的修饰位点磷酸化,乙酰化,泛素化进行鉴定。对蛋白质结构的研究可以有助于深入理解其功能机制,也可以帮助进行药物筛选和设计思路优化。
2. 分析方法和基本原理
2.1. 蛋白质组学定性原理
随着高效液相分离技术(HPLC)和静电场轨道阱(Orbitrap)质谱技术的发展,液相色谱串联质谱(LC-MS/MS)成为目前蛋白质组学分析的主要技术。其鉴定蛋白质的基本步骤(bottom-up):收集样本后进行总蛋白质提取→消化切割蛋白为多肽片段→HPLC分离→分级进入MS电场进一步离子化→MS获得各离子质荷比和峰型信息→软件计算氨基酸组成→数据库检索比对获得蛋白质的定性和序列信息。
2.2. 同位素标记定量原理
基于LC-MS/MS技术的蛋白质组定量技术一般分为标记法和非标记法两种类型。目前常用的标记法有:iTRAQ(体外)、TMT(体外)、SILAC(体内)三种基于同位素标签进行半定量的方法。以常用的iTRAQ蛋白质组学定量为例:iTRAQ是由8种(113/114/115/116/117/118/119/121)同位素标签组成,在实验过程中将8例不同样品分别酶解成多肽片段→分别标记8种同位素标签→将8例标记好的多肽样品混合成1例总样品→进入LC-MS/MS分析系统→二级MS阶段iTRAQ平衡基团发生中性丢失,在低质量区产生多个报告离子→计算各报告离子峰面积,获得同一肽段不同样品间的相对丰度差异比值→加权计算肽段丰度获得总蛋白质相对定量值。
2.3. Label Free定量原理
蛋白质非标记定量技术(Label Free),是直接通过液相色谱质谱(LC-MS)技术结合复杂的数据分析方法对蛋白质酶解肽段进行半定量检测的技术。目前Label Free主要的数据分析方法是利用Maxquant软件,根据一级质谱相关的肽段峰强度、峰面积、液相色谱保留时间等信息进行定量分析的方法;
相比较iTRAQ/TMT等标记方法,Label Free具有特定的技术优势:a. 检测起始样本量少; b. 前处理少,更多保留样本最原始信息;c. 对于低丰度多肽的覆盖程度更高;d. 不受标记试剂盒限制,可进行大批量的样本检测。
2.4. 研究流程
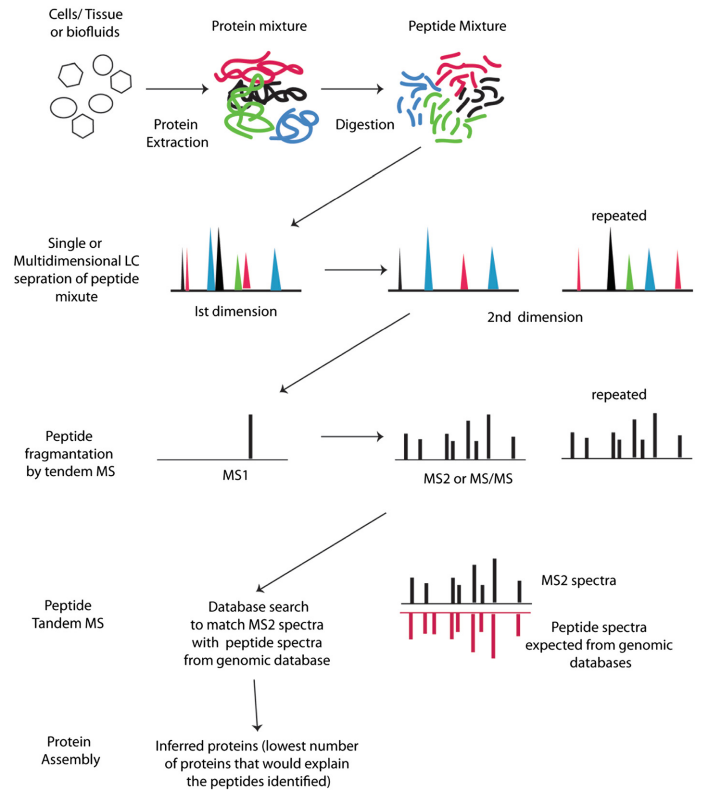
现在目前常用的蛋白质组学研究的分析方法是基于液相色谱-质谱系统(LC-MS/MS)的Bottom-up/Shotgun分析,大致的流程可以分为:
2.4.1. 样品制备:对组织或细胞进行提取分析得到蛋白。样品制备是蛋白质组学研究的第一步,直接影响到后期的研究结果。样品来源不同,制备的方法也有所不同,但都会遵循以下几个原则:①尽可能采用简单方法进行样品处理,以避免蛋白丢失;②细胞和组织样品的制备应尽可能减少蛋白的降解;③尽可能提高样品的溶解度;④防止加入人为修饰。
2.4.2. 样品蛋白分离:通过蛋白酶将蛋白降解为肽段,并利用色谱对酶切后的肽段进行分离。双向凝胶电泳(2DE)是比较早发展的技术,根据等电点和分子量把蛋白在二维水平进行分析,但分辨率较低。高效液相色谱(HPLC)以经典的液相色谱法为基础,引入气相色谱法的理论与实验方法,流动相改为高压输送,采用高效固定相及在线监测等手段发展而成的分离方法,它可以单独使用,或者与质谱仪联用(HPLC-MSM),是目前蛋白质组学中样品分离的主流方法。
2.4.3. 电离和质谱分析:将分离后的肽段加压使其离子化,进行质谱检测,收集信号,得到谱图。
2.4.4. 蛋白鉴定:将质谱结果与数据库进行比对,鉴定出蛋白。
2.4.5. 蛋白定量:根据技术分为标记定量(Label)和非标记定量(Label-free)。标记定量是通过不同化学试剂或同位素对相同肽段进行标记,从而在同一张质谱图中形成具有固定质量差的同位素峰,利用同位素峰从而对特定肽段进行定量分析。目前的技术包括iTRAQ、SILAC、SWATH、ICAT等,通过对一级图谱和二级图谱的分析对蛋白进行定量,具有灵敏度高、定量准确等特点。
非标记定量主要是基于离子流色谱峰(extracted ion current, XIC)的定量算法或谱图计数法(spectral counting, SC)进行蛋白峰度的相对定量。但是对液相色谱分离及串联质谱鉴定的稳定性和重复性要求较高,需要有足够的技术重复以确保结果的可靠性。
2.4.6. 数据分析:将筛选得到的差异蛋白,进行生物信息学分析,对蛋白质组学数据进行多角度的分析和挖掘。
三、蛋白质组学的应用
虽然基因决定蛋白质的水平,但mRNA表达水平并不能代表细胞内活性蛋白的水平,且转录水平的分析不能反应翻译后对蛋白质的功能和活性起至关重要作用的蛋白翻译后修饰过程,如酰基化、泛素化、磷酸化或糖基化等。只有通过对生命过程中蛋白质功能和蛋白质之间的相互作用以及特殊条件下的变化机制进行研究,才能对生命的复杂活动具有深入而又全面的认识。近年来随着各项蛋白质组计划启动实施,短短十几年间,蛋白质组学已经在细胞增殖、分化、肿瘤形成等方面进行了有力探索。这些信息对于全面了解复杂的生命活动规律有着重要的意义。亘安生物的蛋白质分析平台,提供的高通量蛋白质组学分析服务,能够为研究人员提供一站式的蛋白质组学研究方案。
临床研究服务
● 疾病诊断及预后研究
● 疾病动态过程中机制研究
● 机理和调控机制研究
● 疾病标志物的发现筛选
● 用药及预后标志物发现筛选
●药物作用靶点筛选和验证
● 特殊功能蛋白质筛选
基础研究服务
● IP-MS蛋白互作组学分析
● 模式动物/细胞蛋白质组学分析
● 外泌体蛋白质组学分析
● 磷酸化/泛素化/乙酰化/糖基化蛋白质组学分析
● 蛋白质鉴定
● 基于DIA/SWATH的定量蛋白质组学分析
● 基于TMT/iTRAQ的定量蛋白质组学分析
● 基于PRM的靶向蛋白质定量分析
四、交付内容
- 实验报告一份,含具体实验流程及蛋白质组鉴定及定量结果(生物信息学分析)。
- 生物信息学分析内容包括:
- 定性分析:包括肽段、蛋白鉴定结果统计、重复性分析、unique肽段数分布、肽段长度分布、蛋白覆盖度分布;
- 定量分析:包括肽段、蛋白定通量统计、差异蛋白筛选、蛋白丰度比值分布、差异蛋白表达量层次聚类分析;
- 蛋白质功能注释分析:包括GO分类;COG注释;Pathway通路分析;
- 差异蛋白功能富集:包括对差异蛋白GO富集分析;差异蛋白Pathway通路分析;
- 差异蛋白网络互作分析;
- 蛋白质结构域预测等。
参考文献
[1] Bhargava Maneesh, Higgins LeeAnn, Wendt Christine H, et al. Application of clinical proteomics in acute respiratory distress syndrome.[J]. Clinical and translational medicine, 2014,3(1).
[2] Graves Paul R, Haystead Timothy A J. Molecular biologist's guide to proteomics.[J]. Microbiology and molecular biology reviews : MMBR, 2002,66(1).
